[вернуться к содержанию сайта]
С точки зрения ядерной физики.
Совершенно неожиданно семейство лантаноидов привлекло внимание учёных в 1932 г., когда Хевеши открыл, что самарий обладает естественной α-активностью. До того времени считалось, что к α-распаду склонны лишь тяжёлые элементы конца периодической системы, начиная с полония. Быть может, этот факт оказался первым сигналом того, что и в области, подвластной уже не химии, а ядерной физике, удивительное семейство сможет оказаться не менее удивительным.Это подтвердилось более поздними открытиями.
В природе обнаружено 55 изотопов редкоземельных элементов, более 150 радиоактивных изотопов получено искусственным путём. Из общего количества всех известных изотопов 1/8 часть принадлежит редкоземельным элементам. Пожалуй, только в области трансурановых элементов учёным удалось собрать столь же обильный “урожай” радиоактивных изотопов.
А вот другой любопытный факт: среди 55 естественных изотопов лантаноидов 6 радиоактивных, которые имеют очень большие периоды полураспада. Это лантан-138, церий-142, неодим-144, самарий-147, гадолиний-l52, лютеций-176. Пять природных радиоизотопов приходится на область всего 15 химических элементов. Между тем для 56 элементов, предшествующих редкоземельным, т.е. от водорода до бария, достоверно известно лишь 10 радиоактивных изотопов, существующих в природе.
Вот список природных радиоизотопов редкоземельных элементов с периодами полураспада:
|
Изотопы |
Периоды полураспада (лет) |
|
138 La |
1·1011 |
|
142 Се |
5·1015 |
|
144 Nd |
2·1015 |
|
147 Sm |
1,1·1011 |
|
152 Gd |
1·1014 |
|
176 Lu |
5·1010 |
Как видим, все они имеют очень большую продолжительность жизни.
Подавляющее большинство радиоизотопов лантаноидов, как искусственных, так и естественных, склонны к β-распаду, они испускают либо электрон, либо позитрон. Однако учёные обнаружили и искусственно получили целых 16 изотопов, которым свойствен α-распад. Альфа-активный самарий Хевеши оказался лишь первой ласточкой.
Теперь наличие α-распада у отдельных изотопов лантаноидов уже объяснено теоретической физикой. Всякий а α-распад сопровождается выделением энергии. Величины энергий обычно принято выражать в специальных единицах — мегаэлектронвольтах (МэВ). Энергии большинства α-активных изотопов заключены в интервале 4–10 МэВ. Любопытно, что чем больше энергия α-распада, тем больше вероятность радиоактивного превращения данного изотопа и, следовательно, тем меньше его продолжительность жизни. Наиболее энергичные α-активные изотопы имеют периоды полураспада, измеряемые долями секунды. Долгоживущие изотопы, подверженные α-распаду,
дают обратную картину, их периоды полураспада настолько велики, а энергия α-распада так мала, что само излучение удаётся наблюдать с трудом.Физики-теоретики показали, что изотопы с атомными весами больше 140 в принципе могут считаться способными к α-распаду. Иными словами, изотопы элементов середины таблицы Менделеева уже имеют некоторую вероятность испускания α-частиц. Однако это очень малая вероятность, и периоды полураспада таких изотопов были бы астрономически велики. Даже современная радиометрическая техника оказалась бы бессильной обнаружить их исчезающе слабое α-излучение.
Но тут на помощь приходит одна очень важная закономерность ядерной физики. Учёные доказали, что в мире атомных ядер существует своя периодичность. Они даже построили своеобразную периодическую систему ядер. Её периоды заканчиваются особо устойчивыми ядрами — своего рода инертными газами. Эти ядра (их в ядерной физике называют магическими) содержат устойчивые нейтронные и протонные оболочки, заключающие в себе 2, 8, 20, 50, 82, 126 нейтронов или протонов.
Оказывается, те ядра, которые, как говорят физики, находятся в области 82-нейтронной оболочки (например, содержат 84 нейтрона), обнаруживают повышенную тенденцию к α-распаду. Как раз там и расположены редкоземельные элементы. Поэтому первая вспышка α-активности на протяжении периодической системы появляется именно у них.
Значит, и в области атомных ядер удивительное семейство очень своеобразно.
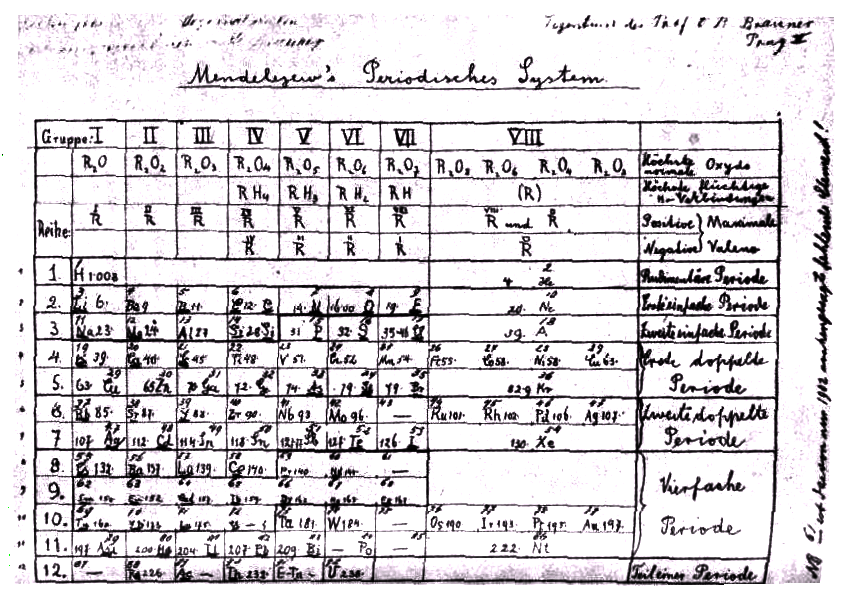
В архиве уже знакомого нам чешского химика Браунера лет 30 назад был обнаружен любопытный документ: выполненный от руки набросок менделеевской периодической системы (см. рис. на с. 82.).

К какому году относится эта табличка? Никаких дат на ней обнаружить не удаётся. Но попробуем сами установить её “год рождения”. Для этого вполне достаточно тех сведений, которые были изложены в предыдущей главе.
У символа каждого элемента написана величина порядкового номера. Уже один этот факт, пожалуй, вполне определённо свидетельствует, что Браунер не мог составить таблицу ранее декабря 1913 г., даже ранее середины 1914 г., когда открытие Мозли стало всеобщим достоянием.
В таблице на месте под № 72 нет символа
Hf; его занимает ещё урбэновский кельтий — Ct. Следовательно, таблица не могла появиться на свет раньше января 1923 г.Итак, мы определили возможные (и весьма вероятные) границы того интервала времени, когда была составлена таблица. Но этот интервал едва ли удовлетворит придирчивого историка науки: он слишком широк — почти 10 лет.
Попробуем его сузить. Определённую помощь нам окажет теперь элемент под № 91. В таблице он записан символом Е-Та (менделеевский “экатантал”). Теперь мы его знаем под именем протактиния — Ра.
Открытие протактиния произошло в конце 1918 г. Имея в виду эту дату, можно предположить, что Браунер начертил таблицу до указанного срока. Интервал, таким образом, сократился и стал менее 5 лет.
Большей точности нам едва ли удастся добиться. Конечно, нам могли бы помочь величины атомных весов (каждый год публиковались специальной Комиссией по атомным весам эти значения, и раз от раза некоторые из них уточнялись в результате новых измерений. Но, к сожалению, в браунеровской таблице атомные веса округлены до целых чисел.
Табличка эта имеет немалый интерес и для историков периодического закона является определённой находкой. Посмотрите, как своеобразно изображена, например, браунеровская интерпериодическая группа редких земель.
Но для нашего очерка куда большую важность представляет другая деталь — короткая надпись по-немецки на полях таблицы:
“NB! 61 ist das von mir 1902 vorhergesagte fehlende Element!”По-русски это значит: “61
— это предсказанный мной в 1902 году недостающий элемент”.Браунер сопровождает эту фразу значком
NB — “заметь хорошо”.Но нет ли здесь какой-то мистификации? Вспомните,
о чём мы рассказывали в первой главе: о том хаосе, который царил долгое время в области редкоземельных элементов. Куда уж здесь отважиться на предсказание существования нового, неизвестного их представителя! Да ещё весьма определённого, чьё место в ряду должно быть между неодимом и самарием?!Нет, Браунер был серьёзным учёным. И если он брался что-то утверждать, то, значит, был в этом достаточно твёрдо убеждён.
Словом, получается, что биография 61-го элемента, о котором далее последует наш рассказ, начинается вовсе не с того момента, когда в руках учёных оказались первые крупицы нового редкоземельного элемента.
Эта биография начинается гораздо ранее. И пожалуй, она сложнее и запутаннее, чем у любого другого элемента периодической системы.
Ведь, в самом деле, редкоземельный элемент между неодимом и самарием несколько раз, казалось бы, появлялся на авансцене истории химии. И почти каждый раз это был выход призрака. По крайней мере, три названия пришлось сменить 61-му элементу, прежде чем он обрёл своё окончательное имя — прометий.
Из всех редкоземельных элементов прометий oбладает весьма удивительным свойством.
Его не существует на Земле!
А потому многолетняя история его поисков — это история заблуждений и ошибок. Может быть, и не стоит о ней рассказывать? Может быть, сказав, что элемента
№ 61 нет в природе, мы слишком рано раскрыли свои карты?Как в ином детективе, где преступник известен самого начала...
Но эта история слишком поучительна, чтобы умолчать о ней.
Снова восьмидесятые годы.
И снова главное действующее лицо — Богуслав Браунер. Друг Менделеева, рьяный сторонник его периодической системы; он хочет помочь Менделееву устранить те трудности, которые стоят перед таблицей элементов.Крепкий орешек предстоит раскусить чешскому химику. Он хочет решить проблему дидима, которая многим исследователям не даёт покоя. Браунер ставит целью получить дидим в пятивалентном состоянии. Удастся это — и вопрос о размещении редких земель в менделеевской системе станет существенно яснее.
Не год и не два работает Браунер. Многие килограммы редкоземельных минералов проходят через его руки. Каждый день он проделывает бесконечные операции разделения и очистки редкоземельных окислов.
Чтобы получить достаточно чистый дидим.
Достаточно чистый? Вскоре Браунер убеждается, что это совсем не так. Полученный образец ему удалось разделить на пять различающихся фракций, которые имели разные молекулярные веса и основность.
Если пересчитать эти значения молекулярных весов на атомные веса входящих в окислы редкоземельных элементов, то мы получили бы такой ряд:
144,32; 145,10; 145,39; 147,10; 149,40.
Как осмыслить полученный результат? В своём отчёте Браунер замечает, что ему удалось “разделить дидим на три компонента: крайние и промежуточные, составляющие смесь крайних”.
Но о пятивалентном дидиме — ни слова.
С таким багажом результатов встретил Браунер 1883 г. По причинам, которые историкам науки выяснить не удалось, он приостановил свои исследования по сортировке дидимовых фракций. И, как вскоре выяснилось, зря. Продолжи он свои работы, и честь расщепления старого дидима на два новых редкоземельных элемента досталась бы ему, а
не Ауэру фон Вельсбаху.Но в науке, как свидетельствует её многовековой опыт, ничто не пропадает зря.
Всё это верно, но читатель вправе спросить: а причём же здесь браунеровское предсказание неизвестного редкоземельного элемента?
Необычный анализ литературных источников.
Когда историк изучает какую-либо проблему, он, как правило, придерживается хронологической последовательности.Но иногда бывает и так: чтобы понять отдалённое прошлое, ему приходится детально разобраться в прошлом менее отдалённом. Путь, конечно, довольно необычный, однако нередко он оказывается полезным.
Трое американских химиков — Джеймс Гаррис, Лео Интема и Джим Гопкинс — в апреле 1926 г. сделали сообщение, что элемент № 61 более не загадка, Дескать, им наконец-то удалось обнаружить этот элемент в природных минералах. Название, предложенное ими было “иллиний”.
Данное событие потом станет предметом нашего подробного изложения, так что здесь примите упоминание о нём за своеобразный анонс.
Но вот что писали, между прочим, американские учёные в своей статье об открытии иллиния: “Не было никаких теоретических оснований для предположения существования элемента между неодимом и самарием, пока закон Мозли не показал возможности идентификации элемента № 61”.
Иными словами, пока периодический закон не обрёл физического смысла, все прогнозы неизвестного элемента в редкоземельной области — просто-напросто пустая трата времени.
Сообщение американцев было изложено в 117-м номере знаменитого лондонского журнала “Природа”, а в следующем, 118-м, появилась короткая заметка Браунера.
Половина страницы журнального текста весьма насыщена информацией. Браунер напоминает:
1) что почти всю свою научную деятельность он посвятил изучению редких земель;
2) что одним из результатов этого было расщепление старого дидима в 1882 г.;
3) что в итоге он пришёл к выводу: “Пробел между неодимом и самарием ненормально широк” (т. е. Браунер имеет в виду большое различие атомных весов Nd и Sm (6, 1).
И в итоге: “Личное знание химии (я думаю, что спектры слишком запутаны) Nd и Sm привело меня к заключению, что между этими двумя элементами существует неизвестный элемент, но все исследования старыми методами были бесплодны”.
Что ж, никакому учёному не безразличен приоритет открытия. Реакция Браунера на выступления американских коллег вполне понятна.
В этой же заметке он чётко указывает, где и когда им впервые был сделан вывод о существовании элемента между неодимом и самарием: в докладе, произнесённом перед собранием Богемской академии наук в Праге в июле 1902 г. То есть спустя полгода после своего исторического выступления в Петербурге относительно идеи “интерпериодической группы редкоземельных элементов”.
Если мы теперь обратим внимание на рисунок, помещённый на с. 29, то бросится в глаза прочерк между символами Nd и Sm.
Однако ни в 1902 г., ни в 1926 г. Браунер нигде не раскрывает нам логической цепи своих умозаключений, которые привели его к предсказанию неизвестной редкой земли. Но убеждённость его в существовании таковой была столь велика, что едва ли можно усомниться: мысль об “эканеодиме” не оставляла его в покое долгие десятилетия.
Как это могло быть в действительности?
Мы и постараемся заняться исторической реконструкцией логической последовательности развития браунеровской идеи. То, что мы собираемся сделать, философы называют мысленным экспериментом.Помимо того что он был одним из виртуозов в области химии редкоземельных элементов, Браунер считался ещё и признанным авторитетом в деле определения и уточнения атомных весов.
Определял он и атомные веса неодима и самария, и слишком большая разница между ними не могла его не насторожить.
Вспомним теперь: работая в начале 80-х годов с дидимом, Браунер разделил его на “крайние” и “промежуточные” фракции. “Крайние”, как это он выяснил позже, представляли собой чистые неодим и самарий. А “промежуточные”? Смеси неодима и самария в разных пропорциях или смеси этих элементов с неизвестным? Браунер скорее всего склонялся в пользу второй возможности.
И, сопоставив это обстоятельство с необычно большой разницей в атомных весах Nd и Sm, Браунер не мог не прийти к выводу о существовании пробела между этими элементами.
Но в столь пресные рассуждения всё же подбросим зёрнышко перца: ведь Браунер предсказал химический элемент, которого нет в природных минералах. Этого, конечно, не знал и не мог знать Браунер, когда впервые предал гласности свою идею в 1902 г. Этого не знали (и никто об этом не догадывался) в 1926 г. Гаррис, Интема и Гопкинс, провозгласившие открытие иллиния.
Вот первый пример предсказания элемента, которого нет!
Неуловимый шестьдесят первый.
Странная судьба бывает у иных идей. После своего доклада в Богемской академии Браунер вплоть до 1926 г. нигде и никогда не вспоминает о своём предсказании (если не считать таблицы, обнаруженной в его архиве). Даже более того, когда в мае 1908 г. он предлагает новый вариант размещения редкоземельных элементов в периодической системе (временно отказываясь от “интерпериодической” гипотезы!), прочерк между неодимом и самарием исчезает.Но означает ли это, что вместе с тем исчезает и уверенность чешского химика в существовании “эканеодима”? Едва ли. Вот его слова, произнесённые на обсуждении нового предложения: “Весьма возможно, неодим окажется сложным. Этот скачок от Nd-144 до Sm-150 кажется мне подозрительно большим”.
В 1914 г. строгие физические исследования, проведённые Мозли, доказывают, что порядковый номер неодима равен 60, а самария — 62. Следовательно, с этого момента искать и найти элемент № 61 становится для химиков делом чести.
Однако именно тут и оказывается уместным задать вопрос: а почему, собственно, этот элемент не был обнаружен ранее? Ведь все прочие редкоземельные элементы удалось извлечь из земных минералов. И вот ещё любопытный факт: элементы первой половины семейства, т. е. цериевой группы, в природе распространены в большей степени, чем элементы иттриевой группы. Стало быть, апелляция к возможной “редкостности” элемента № 61 не имеет должной силы?!
Пусть из-за каких-то неведомых ещё закономерностей природы 61-й элемент есть редчайший из редких, и потому “острота зрения” химического анализа ещё недостаточна для его обнаружения.
Пусть, далее, — опять же вследствие неких таинственных закономерностей — свойства элемента № 61 резко отличаются от свойств его собратьев, и в итоге пытаться искать его следует вовсе не в редкоземельных минералах.
Вот, так сказать, две зацепки для “объяснения отсутствия”.
Два немецких химика — Вильгельм Прандтль и его молодой ассистент Арнольд Гримм, пожалуй, одними из первых предприняли в 1924 г. тщательный поиск “эканеодима”. С помощью рентгеноспектрального анализа (так хорошо зарекомендовавшего себя при открытии гафния) они изучили более 50 препаратов редкоземельных элементов. Спектральную картину “неизвестного” можно было рассчитать по закону Мозли. Однако ни один из спектров изучаемых образцов не показывал ничего даже отдалённо близкого. Не было ни следа, ни намёка на элемент № 61. Свою неудачу исследователи облекли в довольно глубокомысленные рассуждения, и их мы считаем весьма полезным процитировать: “Причина того, что, несмотря на систематические поиски, не найдено следов № 61, достойна внимания и едва ли случайна. Можно заключить, что по своему химическому характеру элемент № 61 или не относится к металлам редких земель, или же вообще не существует”.
Сказав “А”, следовало произнести “Б”. Прандтль и Гримм после своего “глубоко идущего” заключения отваживаются и на определённое обобщение. Вот на с. 90 фрагмент периодической системы в их изображении. В седьмой группе, кроме марганца, все элементы — неизвестные. И следует вывод: “...Возможно, что существующие пробелы 43, 61, 75, 93 периодичны, и может случиться, что они никогда не будут заполнены”.

Боровская теория строения атомов похоронила гипотезу о невиданной химической самобытности элемента № 61; ничем сколь-либо заметным не мог он отличаться от своих редкоземельных собратьев.
Оставалась гипотеза исключительной редкостности или же полного отсутствия. Ни опровергнуть, ни доказать её было нельзя. Незамеченным осталось брошенное вскользь замечание химика Иды Ноддак-Такке о возможной радиоактивности “эканеодима”.
Что бы там ни было, но он оставался неуловимым.
И тут грянул 1926 год.
Дата установки: 16.
02.2009